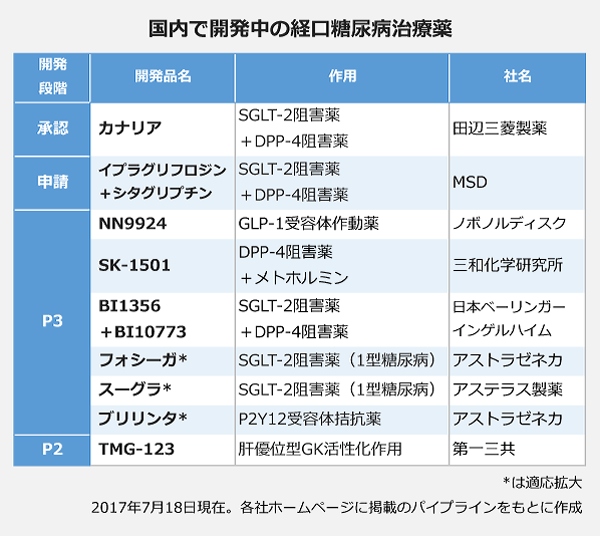
患者数の増加と新薬の登場で市場拡大が続く糖尿病治療薬。一大市場を形成したDPP-4阻害薬や、新規作用機序で注目を集めたSGLT-2阻害薬など、数年前までは新薬開発が活発な領域でしたが、これらに続く新薬候補は相次いで開発中止に。開発競争は一転して下火となりました。
代わって製薬各社が狙いを定めるのが、糖尿病の合併症の中でもアンメット・メディカル・ニーズの高い糖尿病性腎症。バイエル薬品やアッヴィ、第一三共などの新薬候補が開発の後期段階に入っています。
GPR40作動薬など相次いで開発中止に
クインタイルズIMSによると、2016年度の国内の糖尿病治療薬市場は薬価ベースで5260億円(前年度比1.5%増)となりました。薬効別では抗がん剤(9746億円、14.5%増)に次いで2番目の規模。DPP-4阻害薬の登場で市場は一気に膨らみました。
市場拡大を牽引してきたDPP-4阻害薬は、09年12月に「ジャヌビア/グラクティブ」が発売されたのを皮切りに、13年7月までの3年半余りの間に7成分8製品が相次いで発売されました。
次世代の糖尿病治療薬として期待されたSGLT-2阻害薬も、6成分が激しい開発競争を展開。ファーストインクラスとなった「スーグラ」は14年4月に発売され、翌月には「フォシーガ」と「アプルウェイ/デベルザ」、「ルセフィ」が発売。同じ年の9月には「カナグル」、翌年2月には「ジャディアンス」と、1年足らずの間に6成分7製品が市場に登場しました。
武田、アステラス、第一三共などが開発中止
ところが、これらに続くはずだったGPR40作動薬など新規作用機序の新薬候補は開発中止が相次ぎました。
武田薬品工業は13年12月、2型糖尿病を対象に日米欧で臨床第3相(P3)試験を進めていたGPR40作動薬ファシグリファムの開発を中止。同剤の投与で肝機能障害を起こす可能性が判明したためでした。日本たばこ産業が国内外でP2試験を行っていたGPR40作動薬JTT-851も、今年2月に開発中止が発表されました。
GPR40作動薬と似た作用機序で開発が進んでいたGPR119作動薬も、アステラス製薬が13年に、第一三共が今年、それぞれ開発の中止を発表。アステラスは「P1試験の結果および他剤との競合状況などを総合的に勘案した」、第一三共は「所期の目的を達成しなかったため」とその理由を説明しました。
GPR40とGPR119はいずれも、膵臓に存在するGタンパク質共役受容体の一つ。これに作用するGRP40作動薬やGPR119作動薬はグルコース濃度依存的にインスリン分泌を促し、低血糖や膵疲弊を起こしにくいと期待されていました。
ノボの経口GLP-1はP3 帝人の新薬はP2に
GPR40作動薬やGPR119作動薬の開発中止で、パイプラインに残る経口糖尿病治療薬の新薬は、帝人ファーマのTMG-123、ノボノルディスクファーマのNN9924などわずか。現在は配合剤の開発が中心になっています。
帝人ファーマが自社創製したMTG-123は、肝優位型GK活性化作用と呼ばれる作用機序を持ち、現在、2型糖尿病を対象にP2試験が進行中です。同社によると、1日1回投与で、腎機能が低下した患者でも用量調整の必要性が低く、薬物相互作用の懸念が少ないなどといったメリットが期待できるといいます。
ノボのNN9924は経口のGLP-1受容体作動薬です。GLP-1受容体作動薬としてはすでに、複数の企業が注射剤を製品化していますが、経口剤となれば初。現在、国内外でP3試験が行われています。
配合剤では今年7月、田辺三菱製薬のDPP-4阻害薬「テネリア」とSGLT-2阻害薬「カナグル」の配合剤「カナリア」が承認。MSDも「ジャヌビア」と「スーグラ」の配合剤を5月に申請しました。「トラゼンタ」と「ジャディアンス」の配合剤(日本ベーリンガーインゲルハイム)もP3試験が進行中です。
糖尿病性腎症 開発後期に複数品目 SGLT-2の適応拡大も
糖尿病治療薬の開発が下火となる中、開発のターゲットは合併症の一つである糖尿病性腎症に移っています。
糖尿病性腎症は進行すると腎不全になり、治療法は人工透析か腎移植に限られます。日本透析医学会の調査によると、糖尿病性腎症を原疾患とする透析患者は増加しており、2015年末時点では約12万人。透析患者全体の38%を占めました。
糖尿病性腎症または糖尿病を伴う慢性腎臓病を対象に開発が進んでいる新薬候補では、バイエル薬品のフィネレノンとアッヴィのアトラセンタンがP3試験を実施中。第一三共のエサキセレノン(P2b)、スコヒアファーマのTAK-272(同)なども後期段階に入っています。
このうち、バイエルのフィネレノンと第一三共のエサキセレノンは、MR受容体拮抗薬と呼ばれる新規作用機序の薬剤。第一三共によると、腎臓でのナトリウムの再吸収を促進するアルドステロンの受容体に作用し、アルドステロンの結合を阻害することで臓器保護作用を示すといいます。
アッヴィのアトラセンタンは、肺高血圧症治療薬としても別の成分が承認されているエンドセリン受容体拮抗薬。TAK-272は武田薬品が開発していましたが、重点領域の見直しにより、産業革新機構などと共同で設立したスコヒアファーマが開発を引き継ぎました。
SGLT-2阻害薬の適応拡大も開発が進みます。田辺三菱の「カナグル」と日本ベーリンガーインゲルハイムの「ジャディアンス」はP3試験が進行中。アストラゼネカの「フォシーガ」もP2/3試験の段階にあります。