
新型コロナウイルスの拡大で一気に加速すると言われているデジタルトランスフォーメーション(DX)。テレワークが進み、デジタルチャネルを通じた営業活動が広がるなど、デジタル化が遅れていると言われる製薬業界にも変化が見え始めました。製薬業界では今、DXに対してどのような動きがあり、その先にはどんな世界が待っているのか。デロイト トーマツ コンサルティングのコンサルタントと議論します。(連載の全記事はこちら)
コロナ禍で高まる注目
前田雄樹(AnswersNews編集長):新型コロナウイルス感染症(COVID-19)のパンデミックは、医薬品の臨床試験にも大きな影響を及ぼしています。移動の制限などによって、多くの臨床試験が患者の新規登録を一時的に中断するといった対応を余儀なくされました。そうした中、臨床試験の「バーチャル化」や「分散化」にあらためて注目が集まっています。
松原大佑(デロイト トーマツ コンサルティング・マネジャー):「Decentralized Clinical Trial」(分散型臨床試験、DCT)は、患者さんが治験実施施設を訪問する頻度をなるべく少なくすることで、臨床試験の地理的・時間的な制約を取り払うもので、「バーチャル臨床試験」(VCT)などとも呼ばれます。
2011年、米ファイザーが完全バーチャルの「REMOTE試験」を行い、センセーショナルな形で世の中に認知されましたが、当時はまだ課題が多く、なかなか広がりませんでした。その後、米サイエンス37のようなトータルでDCTシステムを提供するスタートアップが登場し、より現実的なものとして実用性が高まってきたところで、COVID-19のパンデミックが重なり、今後は一気に取り組みが進んでいくとみられています。
DCTの実現に必要な各種ツールは、現在ではCROを含むさまざまなプレイヤーから提供されていますが、これらのベンダーに話を聞いてみると、COVID-19の影響で想定よりもはるかに多くの引き合いがあるようです。COVID-19が収束したとしても、従来型の臨床試験に完全に戻ることは考えにくく、今後もバーチャル化・分散化は続いていくと思っています。
前田:DCTと一口に言っても、実はさまざまな要素がありますね。
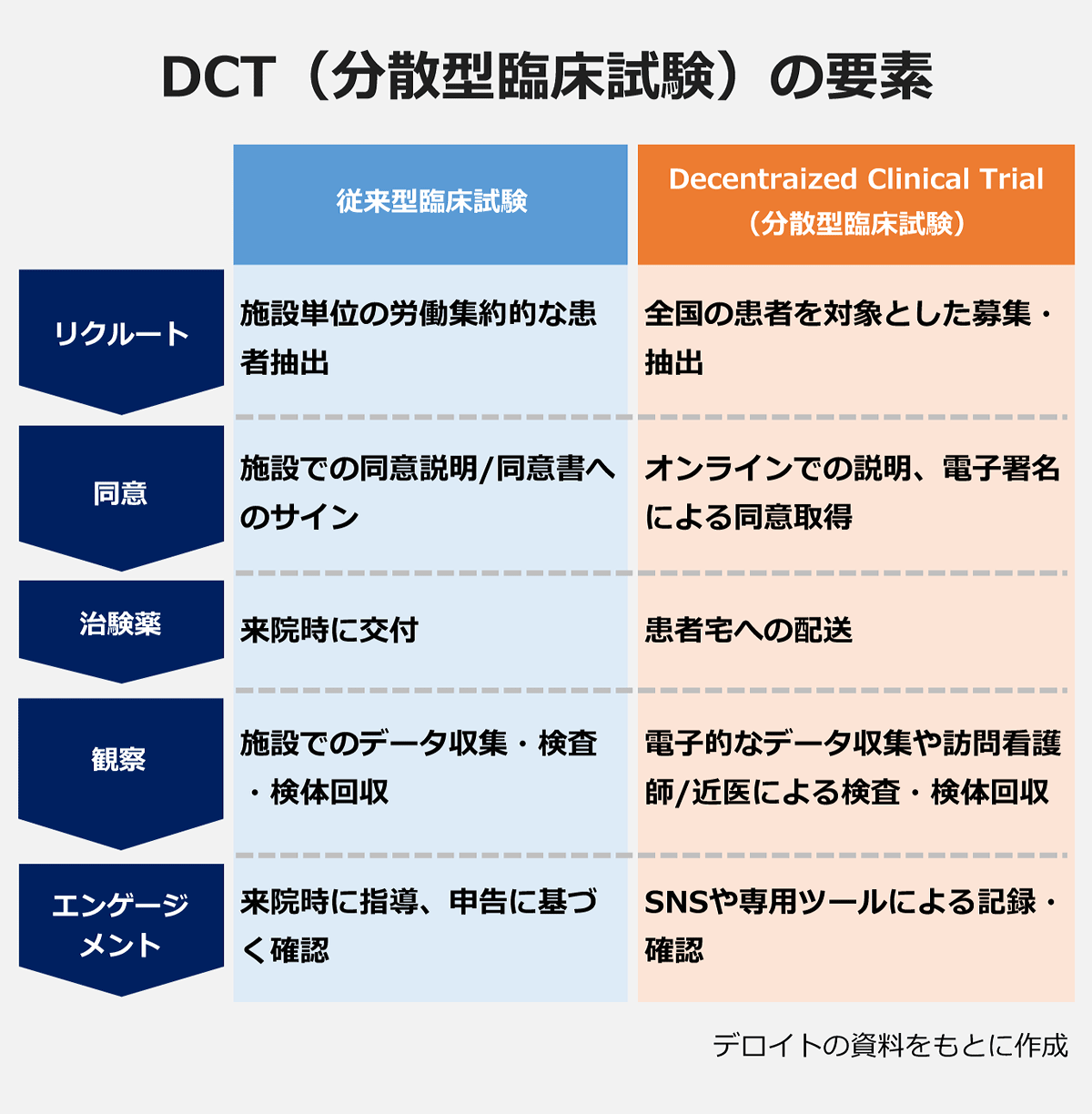
松原:分散化を実現するためのアプローチは複数あって、世間からDCTと認知されている試験は、複数のソリューションの複合体のようなものになっています。すべてのプロセスを分散型で行っている試験はまだ数が限られますが、部分的に患者さんの訪問を減らす要素を取り入れながら行われているのが現状です。
DCTの要素としては、▽オンラインを通じた被験者の募集▽電子的な同意説明・同意取得▽被験者宅への治験薬の配送▽電子的なデータ収集や訪問看護師・近隣医療機関による検査・検体回収▽専用のエンゲージメントツールによる確認やフォロー――などが挙げられます。
少し古いデータになりますが、米国では、臨床試験のおよそ7割が、リクルートメントの遅れによって試験終了が当初の計画から遅延しているというデータもあります。地理的・時間的な制約を取り払うことで、これまで参加が難しかった患者さんにも試験に参加してもらうことができれば、リクルートにかかる時間を短縮することができる。治験実施施設も集約できる可能性があり、試験のコスト削減も期待できます。
期待値高いデジタルバイオマーカー
前田:デジタル技術を使うことで、オンサイトビジットでは取れなかったデータを収集できることもメリットとして挙げられます。ウェアラブル端末を使って日常の活動を測定し、運動機能に対する効果を評価する、みたいな。
松原:デジタルバイオマーカーやデジタルエンドポイントは必ずしもDCTに必要な要素というわけではありませんが、製薬企業の期待値は非常に高いですよね。従来型の臨床試験では、例えば、訪問時に病院の中で歩行テストのようなことをやったりもしますが、患者さんのその日の体調によって結果が違ってしまうこともある。そういったことを極力排除し、日常生活の中でデータを取ることで、有効性や安全性をより正しく、よりロバストに評価できるようになるのは非常に大きいと思います。
増井慶太(デロイト トーマツ コンサルティング・執行役員):6分間歩行試験(6MWT)など、動作や歩行の計測には、定量性を高めたりデータポイントを拡充したりすることが求められるようなものもあるかと思います。子どもの患者さんだと、親のモチベーションによっても結果が変わってくることもあり、そういう疾患はデジタルバイオマーカーと相性がいい。
松原:症状の出方が日によって大きく変わるような疾患でも、デジタルバイオマーカーの活用は大きな機会になるのではないかと思います。そうした疾患の場合、来院時の定点的な測定だけでは症状の波に飲まれて効果を正しく捉え切るのが難しいので、日々自宅で測定できるということが非常に重要になります。
DCT導入に「3つの壁」
前田:日本の臨床試験はこれまで、「紙」や「対面」を重視する慣行が根強く残っており、海外と比べて非効率だと指摘され続けてきました。一足飛びに分散化というのも、なかなか難しそうな気もします。
松原:DCTの導入には、「テクノロジーの壁」「規制の壁」「心理の壁」という3つのハードルがあると考えています。
1つ目のテクノロジーについては、使えるツールとしてはすでに一通り揃っています。ただ、どんなタイプの試験にどんなツールを使うのが良いかというナレッジが業界全体で見るとまだ十分でないので、各社での判断が難しいのが現状です。さらに、デジタルエンドポイントを使うとなると、デバイスや指標の開発と評価が必要になります。これにはそれなりの時間がかかりますし、まだ実績も少ないので、手探りでやっていくしかない状況です。
2つ目の規制ですが、これは国や地域によって異なります。日本の場合、同意説明は対面で行うということになっていて、完全にバーチャルで同意を取得するのは難しい状況です。治験薬についても、メーカーから直接配送することはGCPで認められておらず、実施施設を経由する必要があります。
最もハードルが高いと感じているのが、3つ目の心理の壁です。臨床試験をオペレーションする現場からすると、時間的な制約がある中で新しいものを取り入れるのが難しい。企業のマネジメント層にも「ツールのトラブルでデータが取れないと失敗のリスクが高まるんじゃないか」とか「本当にメリットがあるのか」といったように懐疑的な人もいます。新しいやり方にマインドをシフトしていくというところに、まだ壁があると感じています。
増井:ドラッグ・ラグやデバイス・ラグは解消されても、デジタル・ラグは残っています。COVID-19によって進んではいくと思いますが、海外との差は大きいので、思い切った取り組みが期待されるところです。
DCTに限らずですが、DXの根本課題はチェンジ・マネジメントです。テクノロジーの議論ではなく、人のマインドや行動をどう変えていくか。なかなか一気には進まないと思うので、例えば小規模な試験とか、メディカル部門のエビデンス構築のようなところから始まっていくのではないでしょうか。一気にやって大コケするより、成果と費用が見えやすいような部分から進んでいくと見ています。
松原:どこから着手すべきかということについては、私も同意見です。試験によっても課題は違いますので、確実にメリットが得られそうなところから始めて、そこから展開を広げていくのが望ましいと思っています。承認後の長期フォローアップなども、比較的やりやすいところではないでしょうか。
DCTはメリットも大きいですが、リスクがないわけではありません。トラブルは起きるものなので、一過的にはインテンスなモニタリングやチェックが必要になってくる場合もあります。DCTをやろうとすれば、オペレーション上で対応しなければいけないことも出てくるので、それを組織としてやりきれるかというのも論点になってきますね。
変わるモニタリングのあり方
前田:CROのビジネスやCRAの働き方も変わりそうですね。
松原:CROのビジネスは当然変わるでしょうね。モニタリング業務のボリュームがどうなるかはわかりませんが、オンサイトで行う業務は確実に減っていくと思います。一方で、ウェアラブル端末やePROから細かいタイムラインでデータが入ってくるようになると、今度はそれをセントラルで細かくチェックする必要が出てくる。必ずしもモニターの仕事が楽になるというわけではないと思いますが、モニタリングのあり方は確実に変わっていくでしょう。
増井:現場のモニターからもデジタル化の要望は高いように思います。出張も多く、サイトビジットも大変なので、効率化していきたいというのが全体的なトーンのように感じています。
松原:ただ、日本の医療機関ではeSourceができるところは少ないのが現状です。効率化の観点では、医療機関側のデジタル化も同時に進めていかないと、メリットとしては打ち出しにくい。
接近する臨床試験と実臨床
前田:分散化やバーチャル化の動きも踏まえた上で、臨床試験のあり方は今後、どうなっていくと見ていますか?
松原:デジタル化が進展していくと、将来的には実臨床と臨床試験の垣根は取り払われ、治験のためだけにデータを集めるということが少なくなっていくのではないかと考えています。臨床試験の中であるデータを集めることが患者や医療従事者にとってベネフィットがあるのであれば、それは実臨床の中でも継続して行われるべきですし、それによって誰かが収益を得るようなビジネスモデルも可能なのではないでしょうか。
増井:臨床試験と実臨床の融合は、賛否両論あるし、多くのチャレンジもあると思います。一方、現行のRCTに対しては「小規模・実験的・計画的」ということで実臨床を反映していないという議論もあり、段階的に実臨床のデータもうまく取り込みながら開発の精度を上げ、コストを下げるという世界になっていくのでしょう。
薬剤軸にソリューション提供
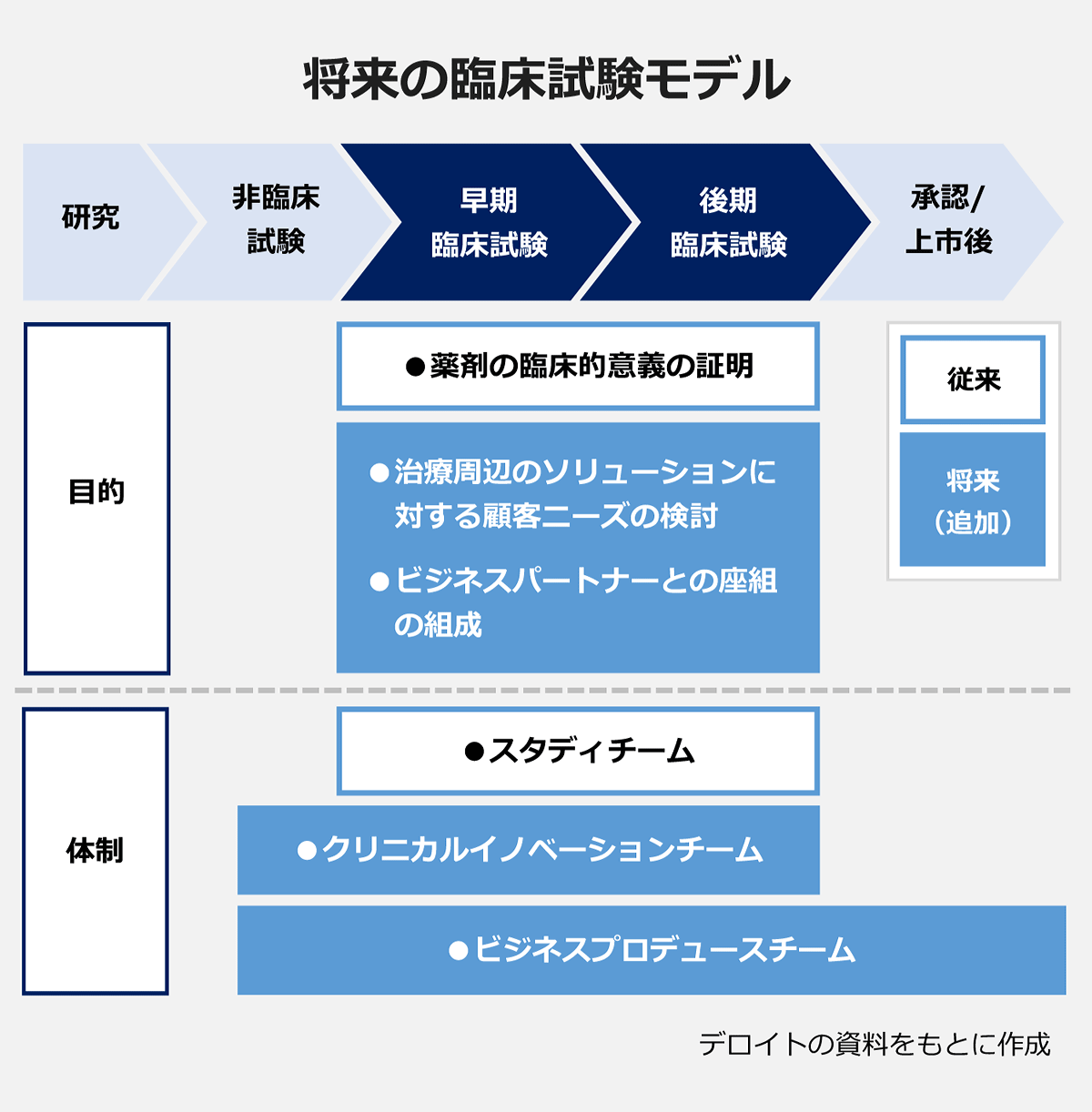
前田:臨床試験という場が、単に薬剤の有効性・安全性を確認する場ではなく、新たなビジネスを生み出す場になっていくかもしれませんね。
松原:薬剤の有効性・安全性を確認することに加え、治療周辺のソリューションに対する顧客のニーズを検討したり、将来に向けたビジネスパートナーとの座組を組成したりといったこともできるでしょう。そのためには、薬剤単体ではなく、それを軸に実臨床の場にどんなサービスを提供していくのかということを、化合物が研究から上がってくる段階から考えるためのチームが必要になると思います。
増井:製薬企業としては、パイプラインだけでなく、臨床試験のようなオペレーションのレイヤーでもイノベーションを起こすことで、20年後の世界でも生き残っていける、強みを持っていられる、そういう会社も出てくるかもしれませんね。

増井 慶太(ますい・けいた)=写真左。デロイト トーマツ コンサルティング合同会社執行役員/パートナー。米系戦略コンサルティングファーム、独系製薬企業(経営企画)を経て現職。「イノベーション」をキーワードに、事業ポートフォリオ/新規事業開発/研究開発/製造/M&A/営業/マーケティングなど、バリューチェーンを通貫して戦略立案から実行まで支援。東京大教養学部基礎科学科卒業。 松原 大佑(まつばら・だいすけ)=写真右。デロイト トーマツ コンサルティング合同会社マネジャー。京都大理学部卒業後、同大大学院生命科学研究科で博士号を取得し、アカデミアで研究に従事。現職ではR&D領域のテーマに数多く携わり、AI/ML/DLの活用を含むデジタルトランスフォーメーションに関する取り組みにも幅広い知見を有する。 |










