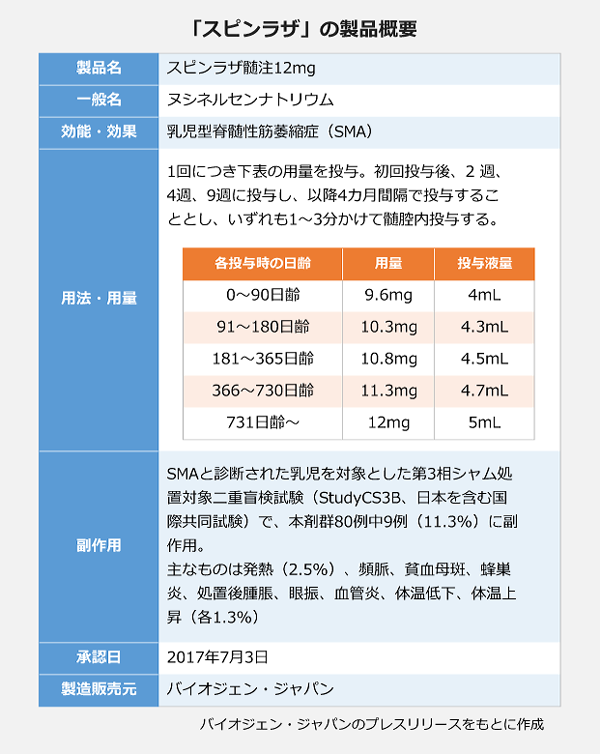
国内初のアンチセンス核酸医薬として話題を呼ぶバイオジェン・ジャパンの脊髄性筋萎縮症治療薬「スピンラザ」。日本では今年7月、申請からわずか7カ月で承認を取得し、8月中にも発売となる見通しです。
難病に対する画期的新薬であることはもちろん、注目されるのは薬価。先に発売された米国では1瓶1000万円を超える値段がつきましたが、日本では932万円となりました。米国や欧州の価格は下回ったものの、最初の1年は5592万円、それ以降は年間2796万円の費用がかかる計算です。
申請からわずか7カ月のスピード承認
厚生労働省は7月3日、バイオジェン・ジャパンの脊髄性筋萎縮症(SMA)治療薬「スピンラザ」(一般名・ヌシネルセンナトリウム)を承認しました。疾患に関係するタンパク質をつくるRNAを標的とするアンチセンス核酸医薬としては国内初。通常、新薬の承認審査には12カ月程度かかりますが、スピンラザは昨年12月の申請からわずか7カ月でのスピード承認となりました。
SMAは、運動ニューロンの正常な機能を維持するのに必要なSMNタンパク質をつくるSMN1遺伝子(SMN=survival of motor neuron =運動神経細胞生存)の変異が原因。SMNタンパク質がつくられず、脊髄内の運動ニューロンに変性が生じることで、筋肉が萎縮して筋肉量と筋力が低下していく疾患です。
SMAは発症の時期によって0~IVの5つの型(出生後間もなく死亡する0型と、20歳以降に発症し、生存期間は健康成人と変わらないIV型はまれ)に分類されます。半数以上を占めるI型(生後6カ月ごろまでに発症)では体を動かしたり、自力で座ったりすることができず、呼吸や嚥下といった生命維持に必要な身体機能にも支障をきたします。
日本では指定難病となっており、国内の有病率は推定で10万人あたり0.5~1人。I型は出生2万人に1人前後と言われています。2014年度に特定疾患医療受給者証の交付を受けた人は894人でした。
スプライシング変え正常タンパク質を産生
「スピンラザ」が標的とするのは、SMN1とよく似た構造を持つ重複遺伝子のSMN2。SMN2もSMNタンパク質をつくりますが、そのほとんどは不完全なもので、通常では意味のあるものにはなりません。スピンラザはこのSMN2のmRNA前駆体に結合し、スプライシング(DNAから転写された遺伝情報から不要な部分を除去する過程)を変えることで、正常なSMNタンパク質の産生を増やします。
今回、スピンラザが承認を取得したのは乳児型SMA。承認の根拠となった乳児型SMA対象の国際共同臨床第3相(P3)試験「ENDEAR」の中間解析データによると、運動機能を改善した患者の割合はシャム(擬似的)処置群で0%だったのに対し、スピンラザ投与群では41%(最終解析では51%)。この中には「頭を上げる」「寝返る」「座る」「立つ」などの運動マイルストーンを達成した乳児もいたといいます。
薬価は1回932万円、最初の1年で5592万円
「乳児型SMAに苦しむ日本の患者と家族に治療薬を届けられることを嬉しく思う。臨床試験で示された有効性と安全性のプロファイルに基づき、スピンラザがこの重篤な疾患を抱える患者に有意義な影響を与えることになると信じている」
承認取得を受け、バイオジェン・ジャパンの鳥居慎一社長はプレスリリースでこうコメントしました。これまで根本的な治療法が存在しなかったSMA。患者・家族の期待は高まります。
米国やドイツを大きく下回る
国内初のアンチセンス核酸医薬という画期性や治療に与えるインパクトもさることながら、注目されるのが薬価。2016年12月に申請からわずか3カ月で承認されたことが話題となった米国では1瓶1620万円、今年5月に承認された欧州(ドイツ)では1297万円の値段がつきました。
日本では8月23日に開かれた中央社会保険医療協議会の総会で1瓶932万424円とすることが決まりました。年間の薬剤費は、投与回数の多い最初の1年は5592万円、それ以降は2796万円となる計算。高額な薬価となりましたが、米国やドイツの価格は大幅に下回りました。もちろん、高額療養費制度があるため、患者の負担は限定的です。
スピンラザの薬価は原価計算方式で算定されました。▽新規作用機序の薬剤である▽臨床試験で運動機能の有意な改善が認められた▽先天性の遺伝子変異による致死的な脊髄性筋萎縮症に対する初の医薬品である――ことなどが評価され、営業利益率に35%の加算が付きました。これは、2015年9月に薬価収載された免疫チェックポイント阻害薬「オプジーボ」(加算率60%)、11年7月収載の抗がん剤「ハラヴェン」(40%)に次ぐ高い加算率です。
スピンラザは今年9月に乳児型以外のSMAへの適応拡大が予定されており、今回の薬価は乳児型以外も含めた予測投与患者数を加味して算定されました。ピーク時の投与患者数と年間売上高は、乳児型が294人で97億円、それ以外が120人で22億円と見込まれています。
核酸医薬は次世代のバイオ医薬品として期待されており、日本企業では日本新薬と第一三共がデュシェンヌ型筋ジストロフィー向けのアンチセンス核酸医薬を開発中。日東電工は自社創製した肝硬変などに対する核酸医薬の開発で米ブリストル・マイヤーズスクイブと提携しました。スピンラザの承認は核酸医薬の開発に弾みをつけそうです。